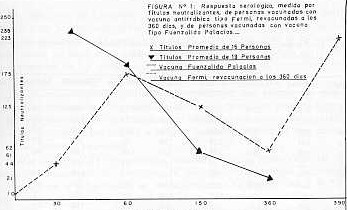
|
Veterinaria Tropical. 1: 41-50. 1976 VALORES SEROLÓGICOS OBTENIDOS POR Titulación DE ANTICUERPOS RABICOS EN SUEROS HUMANOS ELVIA
DE MOGOLLÓN*, HORACIO DELGADO CH.*, MARTÍN BARROETA F.**,
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
INTRODUCCIÓN En nuestro estado actual de conocimientos, es difícil correlacionar el valor de anticuerpos neutralizantes, con el grado de protección conferida por un determinado antígeno, (1,3,4,7,9,10) pero siendo la técnica de neutralización el método más generalizado para detectar anticuerpos se procedió a cuantificar los títulos de anticuerpos de un grupo de personas, siguiendo el método de KOPROWSKI y JOHNSON ( 12 ), modificado por ATANASIU (2 ). Al no recomendarse para humanos la aplicación de vacunas vivas, se ha generalizado el uso de vacunas inactivadas, ya sea tipo Semple, Fermi, Fuenzalida, o embrión de pato, para inducir una inmunidad capaz de proteger a la persona expuesta. El presente
trabajo surge, como consecuencia de la preocupación por mantener
protegidos a los individuos que trabajan en el laboratorio, en constante
exposición al virus de la rabia, ya sea por inoculación directa o por
riesgo de aerosoles (6). MATERIALES Y MÉTODOS Grupo I Grupo II Corresponde a 19 infantes de marina, quienes habían sido mordidos por vampiros en la Base Naval de Turiamo, Distrito Girardot, Municipio Ocumare de la Costa, Estado Aragua, cuando realizaban maniobras militares. De este grupo
de personas no se pudo obtener suero a los 0 días, solamente a
30-60-150 y 360 días de la última dosis. Vacuna empleada: Grupo I La vacuna tipo Fermi (13) estaba preparada a base de una suspensión de cerebro de carnero, proporcionada por el Instituto Pasteur de París, lote N° 888, conteniendo 25 mg. de material antigénico por dosis de 0,25 ml. inactivado con Betapropiolactona 0,25 por mil. Grupo II La vacuna C. R .L .de FUENZALIDA-PALACIOS (8) consistía de una suspensión de cerebro de ratón lactante, (20 mg. por dosis), en volumen de 2 ml. inactivada con luz ultravioleta y preservada por fenol 1/1.000 y Thimerosal 1/10.000. Estas vacunas habían cumplido, antes de su uso con los requisitos de inocuidad y potencia exigidos por las autoridades sanitarias. Esquema de vacunación: Para el grupo I: 3 dosis de 0,25 ml. c/u a intervalo de 30 días, por vía intradérmica. Para el grupo II: Se siguió un esquema de inmunización (15) que consistió de 2 ml. c/u, una en la mañana y otra en la tarde durante 7 días consecutivos por vía subcutánea. A partir del 8° día, se inyectaron 2 ml. diarios por otros 7 días consecutivos.
Después de 10 días de haber finalizado el primer tratamiento, se aplicó un primer refuerzo a los 24 días de la primera dosis y un segundo refuerzo a los 34 días de la primera dosis. Prueba de Seroneutra1ización: Se utilizó la técnica de KOPROWSKI y JOHNSON (12) modificada por ATANASIU (2). Se empleó la cepa de virus CVS, de un X pase en cobayos jóvenes, sacrificados en estado agónico. Como diluentes se usó agua destilada conteniendo 2% de suero normal, equino, inactivado a 56°C, por 30 minutos. El título infectivo de la suspensión de virus usado se situó entre las diluciones 10-6.4 a 10-6.7. En base a estos datos se tomó teóricamente 40 DL50/0,03 ml. como dosis de exposición frente a los sueros. Básicamente los sueros fueron expuestos frente a valores fluctuantes entre 42 y 100 DL50/0,03. En cada prueba montada la suspensión de virus se tituló nuevamente en las mismas condiciones en que se colocaron los sueros a probar, es decir, se agregaron 0,5 ml. de la dilución correspondiente de virus, en un tubo conteniendo 0,5 ml. de suero normal de pollo, diluido 1/5 y seguidamente se incubaron por 90 min. a 37°C. Animales de experimentación: En las pruebas de Seroneutralización, se escogieron ratones adultos, (Mus musculus domesticus, variedad albino ), con un peso que oscilaba entre 14 y 16 grs. Se inocularon 8 ratones por dilución con 0,03 ml., vía intracraneal y fueron observados durante 15 días. El cálculo del título infectivo del virus y el número de DL50 utilizados, se obtuvo mediante el método de REED y MUENCH (16), determinando la dilución de suero que protege el 50% de los animales inoculados. RESULTADOS En los resultados se puede observar que existen diferencias en la respuesta sérica inmunitaria entre el grupo de personas vacunadas con la vacuna de cerebro de carnero tipo Fermi y el grupo de personas inoculados con la vacuna FUENZALIDA-PALACIOS. Como se puede apreciar en el Cuadro 1 los valores de la respuesta inmunitaria referidos a los títulos neutralizantes del grupo N° I, muestran que con un solo estímulo antigénico se generan títulos neutralizantes que varían entre 1: 5 y 1 : 125 cuando se exponen con una dosis de 42 DL50 de virus. A los 60 y 150 días se pudo observar el efecto de refuerzo de la vacunación, ya que en todos los casos hubo un aumento apreciable de los títulos neutralizantes. No obstante, se nota, que a los 360 días, estos valores, aunque presentes disminuyen en cantidad. Sin embargo, al colocar un refuerzo a los 360 días, se puede notar un aumento apreciable de los títulos neutralizantes. De todas maneras se observa bien el efecto del refuerzo en ambos casos como se ve en la figura N° 1. A los 60 días se nota que un 56% de los vacunados en el grupo N° I aumentan los títulos neutralizantes y que estos títulos se mantienen aun hasta los 150 días ( 93% ) ( ver Cuadro 2) .
Del total de 16 personas vacunadas, 10 de ellas presentan títulos neutralizantes (62,5% ) a los 360 días. La respuesta inmunitaria en el grupo de infantes de marina (grupo N° II) se aprecia en el cuadro N° 3. A pesar de desconocer la actividad serológica de los marinos a los 0 días, se puede muy bien observar que los títulos de anticuerpos neutralizantes generados a los 30 días de la última dosis son muy elevados y que a partir de ese momento los anticuerpos comienzan a descender paulatinamente como se ve en la figura N° 1.
A los 60 días de la última dosis un 41% del grupo mantienen sus títulos pero al contrario de los del grupo I, los títulos comienzan una curva francamente descendente. Ya a los 150 días solamente el 21% mantienen buenos títulos de anticuerpos neutralizantes mientras se nota una marcada tendencia a disminuir los mismos ( 78,9% ) ( ver Cuadro 2) .En este mismo cuadro se muestra que un 84% del total del grupo disminuyen sus títulos pero aun conservando títulos significativos de 1: 25 . En ninguno de los 2 grupos de personas sometidas a estas vinculaciones se reportaron accidentes postvacunales, enfermedad grave o muerte de los mismos durante el tiempo de duración del ensayo. En este estudio no se tomó en cuenta diferencias de sexo o de edad. DISCUSIÓN La utilización de PASTEUR (14) por primera vez de una vacuna antirrábica a un ser humano abrió la ruta al estudio de la profilaxis de la rabia. Es su esquema de vacunación de 14 dosis el que más se ha usado hasta ahora en todo el mundo. Esto puede variar de acuerdo al grado de exposición de las personas a contraer la enfermedad o también de acuerdo a la respuesta inmunitaria del paciente (5, 9,10). Es de considerable importancia correlacionar los valores de anticuerpos neutralizantes y la resistencia que puede tener una persona frente a una infección con el virus rábico; no obstante, los conceptos actuales no están bien definidos debido a la gran variación individual que existe entre las personas expuestas. HELD y Col. ( 11) demostraron recientemente las diferencias en la respuesta inmunitaria de 3 grupos de personas con distintos esquemas de vacunación ya las cuales se les suministró una vacuna de C.R .L . con un bajo valor antigénico, habiéndose encontrado que existe una correlación directa entre el número de personas con respuesta, el nivel de los anticuerpos neutralizantes en el suero, la dosis de vacuna administrada y la proporción de respuesta, la cual fue más alta en el grupo de personas de 5 a 24 años que en los de 25 años o más. Aunque en este estudio no se tomaron en cuenta valores estadísticos ni distinciones por edades, aún se pueden apreciar diferencias entre los dos sistemas de vacunación. Del grupo de 19 personas vacunadas con vacuna tipo Fermi, 3 de ellas habían recibido anteriormente una dosis de vacuna de embrión de pato ya pesar de que no se detectaron anticuerpos significativos a los 0 días de este estudio, la respuesta en ellos fue superior en todo momento a la de las demás personas del grupo. Este hallazgo no difiere de los reportados por otros autores. GREEMBERG y CHILDRESS ( l0) notan en su estudio que 6 de 9 de sus pacientes habían sido vacunados antes de comenzar el tratamiento antirrábico, demostrable esto por la presencia de anticuerpos neutralizantes. En las personas del grupo II, a pesar de que no se conocía su respuesta serológica a los 0 días, se pudo comprobar una elevada actividad serológica a los 30 días de aplicación de la vacuna C. R. L., coincidiendo con las observaciones de HELD y Col. (11) .Esto indudablemente enfatiza la importancia de una vacunación previa en aquellos casos de personas expuestas al virus rábico, haciendo de esta manera muy importante la dosis de refuerzo en caso de nuevas exposiciones. Al comparar los dos grupos y la efectividad de ambas vacunas se concluye que hay diferencias, ya que a pesar de que la tendencia de los títulos de anticuerpos neutralizantes es a disminuir con el tiempo y que al contacto nuevamente con otras dosis de vacuna se observa el efecto de refuerzo como se apreció con la revacunación con la vacuna tipo Fermi a los 360 días, la respuesta serológica en el caso del grupo de personas vacunados con la vacuna tipo Fermi fue siempre un poco mayor que los vacunados con la vacuna C.R.L ., no obstante que la cantidad de antígeno usada con esta última fue seis veces mayor. La vacuna C .R .L . usada en el tratamiento preventivo de los infantes de Marina fue aplicada por el médico sanitarista de la región y fue probada y administrada de acuerdo con los esquemas del Ministerio de Sanidad y Asistencia Social de Venezuela. Es muy posible que el valor antigénico de esa vacuna fuese bajo, pero no lo pudimos constatar ya que su aplicación escapó a nuestro control. RESUMEN En el laboratorio de investigaciones y diagnóstico de la rabia del Instituto de Investigaciones Veterinarias, se procedió a la vacunación y revacunación del personal de laboratorio y otros voluntarios, utilizando una vacuna antirrábica inactivada tipo Fermi, la cual se aplicó de acuerdo a un esquema de vacunación simplificada. Los resultados muestran que 3 dosis por vía intradérmica a intervalos de 30 días con un refuerzo anual, generan una respuesta inmunológica satisfactoria cuando se titulan los anticuerpos neutralizantes. Comparando estos resultados con los obtenidos en un grupo de infantes de Marina, mordidos por quirópteros, y sometidos a una inmunización con 22 dosis de vacuna inactivada tipo Fuenzalida, recomendada por la Organización Mundial de la Salud, se puede establecer diferencias entre los dos sistemas de vacunación. SUMMARY A group of laboratory personnel and volunteers were vaccinated and thethen revaccinated using an inactivated vaccine Fermi Type. The results show that giving 3 intradermic doses within 30 day intervals and one annual revaccination dose, a good inmunological response is achieved as shown by the serum neutralization test.Comparing these results with the one found in a group of Navy Soldiers bit ten by bats and later vaccinated with 22 doses of an inactivated vaccine Fuenzalida Type, demostrates the difference in antibody response between the two vaccines. BIBLIOGRAFÍA 1. ATANASIU, P. Quantitative assay and potency test of antirabies serum, in "Laboratory techniques in Rabies" .2a ed., Ginebra, O. M. S. , 1969. 2. ATANASIU, P. Seminario Int. sobre Producción y Control de Vacunas antirábicas. Buenos Aires, Centro Panam. Zoon, 17-28. Nov. 1969. 3. ATANASIU, P., et al. Rabies neutralizaing antibodies response to different schedules of serum and vaccine inoculations in non-exposed persons. Buul. Wld. Hlg. Org. 14, 593-611. (1956). 4. ATANASIU, P., BAHAMANYAR M., BALTAZARD, M., Fox, J. P., HABEL, K., 4. ATANASIU, P., et al. Rabies neutralizaing antibodies response to different schedules of serum and vaccine inoculations in non-exposed persons: Part II Bull. Wld. Hlth. Org. 17, 911-932. (1957) . 5. CAMPILLO, C ., NÚÑEZ, A. , y LÓPEZ, F. Inmunizacion primaria antirrábica humana con diferentes dosificaciones de vacuna tipo Semple. Sal. Public . Mex. 8, 17-24. (1966) . 6. COÑSTANTINE, C. D. Rabies transmision by air in bat caves. Atlanta, 6a, U.S.A, National Comunicable Disease Center (P.H.S. Publicat 1617) (1967). 7 . FÁBREGA, F. , FUENZALIDA, E. , y RODRÍGUEZ, R .Estudio de los anticuerpos neutralizantes en el suero sanguíneo de bovinos tratados con vacuna antirrábica Zooiatría, VI. (14) 1-9. (1965) . 8. FUENZALIDA, E. y PALACIOS, R. Un método mejorado en la preparación de la vacuna antirrábica. Bol. Inst. Bact. Chile 8; 3-10 (1955) . 9. FUENZALIDA, E. y PALACIOS, R., and BORGOÑO, M. Antirrabies antibody response in man to vaccine made from infected suckling mouse brain .Bull. W.H.O. 30; 431-436. (1964) . 10. GREEMBERG, M., and C1LDRESS, J. Vaccination against rabies with Duck embryo and Semple vacciones. J.A.M.A. 173, 333-337. (1969). 11. HELD, J. R., FuENzALmA, E., L6PEZ, A. H., ARROSSI, J. C., POLES, N.O.R. y SCIVETTI, A. Immunización humana con vacuna antirrábica de cerebro de ratón lactante. Bol. of San. Pan 72, (6) .565-575. (1972). 12. KOPROWSKI, H. and JOHNSON, H. Serie de Monografías. O.M.S. 23,70-75. (1959). 13. LEPINE, P., ATANASIU, P., CAMET, A., VIEU, J. P., y VIALAT, C .Les vaccinations antirabiques a L' Institut Pasteur en 1967 Ann. Inst. Pasteur . 115, 297-301. (1968) . 14. PASTEUR, L. Methode Pour prevenir la rage apres morsure. C. R. Acad. Sci (Paris) 101, 765-772. (1885). 15. Recomendation of the U. S. Public. Health Service. Advisory Committee on inmunization practice. Rabies Prophylaxis, Sept. 1969. 16. REED, L. P. J. , MUENCH, H. A simple method of estimating fifty percent end points. Amer. J. Hyg. 27, 493-497. (1938) . |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||