|
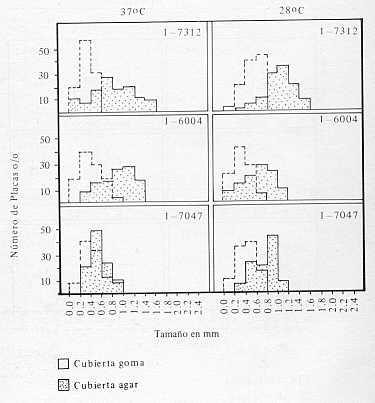
RESUMEN Se estudiaron seis aislamientos del serotipo Indiana (Ind.) y 16 del Serotipo New -Jersey (N.J.), en monocapas de células BHK21. En el experimento se usaron dos temperaturas diferentes (28°C y 37°C) y dos diferentes capas de cubierta (agar y goma). El título determinado por placas no fue afectado por la temperatura ni por la cubierta utilizada. El promedio de tamaño de placa no se diferencia a las dos temperaturas estudiadas, pero sí se diferencia bajo las dos monocapas a las dos temperaturas. Mientras que el tamaño de la placa de cada cepa varía con la temperatura, existe una relación bajo cubierta de agar pero no de goma. La distribución de la variabilidad del tamaño de la placa observado en un histograma, sugiere heterogenicidad de la población en la mayoría de los aislamientos Las cepas del serotipo New Jersey que tenían placas de mayor tamaño, fueron más virulentas para ratones que aquellas cepas que mostraban placas de menor tamaño. Lo inverso fue cierto para aislamiento Ind.; las variantes de placa pequeña de estos virus fueron mas virulentas. INTRODUCCION Las características de crecimiento bajo condiciones controladas en cultivo de células, han sido utilizadas como criterio de diferenciación entre subcepas de ciertos virus ( 9, 16, 29 ). La morfología de la placa ha sido particularmente útil como indicador de diferencias entre cepas, observándose ciertas relaciones entre el tamaño de la placa y la virulencia de un mismo virus para su huésped natural (17, 19, 23, 28, 30). Existen pocos reportes sobre la caracterización del virus de la Estomatitis Vesicular (E.V.), o de diferenciación de serotipos en base a la morfología de sus placas. El objetivo de este trabajo es reportar el uso del método de cultivo celular para distinguir aislamientos del virus de la E. V. en base a tamaño de placa, título modificado por el uso de diferentes medios de soporte y temperatura de incubación. REVISIÓN BIBLIOGRAFICA Wagner (34) reportó dos variantes de tamaño de placa presentes en un aislamiento del serotipo Indiana (Ind.) cuando se cultivó en monocapas de células de embrión de pollo y de células L. Estas variantes no se diferencian significativamente en las propiedades de absorción en células de embrión de pollo y en células L; liberación de células L. infectadas; termostabilidad; crecimiento en presencia de extractos de agar; tamaño de placa; crecimiento bajo condiciones reducidas de bicarbonato, inactivación de infectación por luz ultravioleta y citotoxicidad. Ligeras variaciones pudieron ser demostradas en neutralización y en densidad boyante en gradientes de cloruro de cesio. Los aislamientos Indiana, C. Cocal y Argentina produjeron placas de forma regular de 3 a 4 mm de diámetro. El serotipo Brasil produjo dos tipos distintos de placa, ,una irregular de 1 a 2 mm de diámetro que formaba 80 % de población y otra placa mayor de 3 a 4 mm de diámetro que constituían el resto de la población (8, 31). Tilles (32), comparó los serotipos Cocal, Indiana y New Jersey (N.J.), con respecto a la formación de placas y multiplicación en monocapas de células BHK21 a varias temperaturas. Mientras algunas cepas N.J. e Ind. podían multiplicarse y formar placas hasta una temperatura de 41°C, el virus Cocal sólo podía realizarlo a 39°C. Lauerman (15) y Nizanov (22), describen placas de dos tamaños y sus propiedades biológicas. La patogenicidad de los mutantes de la placa de serotipos N.J. también han sido descritos (26). MATERIALES Y METODOS VIRUS: Los aislamientos fueron obtenidos en veinte brotes de la enfermedad en bovinos, que se presentaron en Colombia durante los años 1971 - 1975. Las localidades de orige n representan las principales zonas ecológicas del país, con altitud es entre 18 y 2.700 metros sobre el nivel del mar y 16 diferentes municipios en 9 de 21 departamentos. CÉLULAS Y MEDIOS DE CULTIVO: La línea de células BHK21 una de las varias células susceptibles, ( 1, 2, 4, 6, 11) fue cedida por el Centro Panamericano de Fiebre aftosa. En nuestro laboratorio estas células fueron cultivadas en medio 199, suplementadas con 0,5 de hidrolizado de lactoalbúmina y con 10 % de suero fetal bovino. El medio de soporte contenía 0,9 % de Ionagar N° 2, u 0,8 % de goma tragacanto y medio 199 2x. El medio fue reconstituido de acuerdo a las instrucciones de los fabricantes, agregándose 1 % de 0,01 M tricina, 10 % de suero fetal bovino y antibióticos (penicilina 100 u/mI y estreptomocina 100 mg/ml). De un stock de bicarbonato de sodio al 7,5 % se adicionó suficiente cantidad para obtener un pH de 7,2. TÉCNICA DE PALANQUEO: Para preparar las bandejas, la monocapa de células cultivadas en frascos ROUX fue lavada dos veces con solución salina buferada fosfatada (PBS) y las células despegadas con una mezcla de 0,8 % tricinal y 0,05 % versene. Las células fueron luego resuspendidas en medio 199 que contenía 10 % de suero fetal bovino, 1 % de 0,01 M tricina y antibióticos, con pH final de 7,2. En cada celda de las bandejas se colocaron 350.000 células, luego se incubaron a 37°C en una estufa sin suministro de C02. El medio fue descartado después de 24 horas de incubación, y se agregó 0,1 ml de la suspensión viral por celda. La absorción se realizó por una hora a 21°C. Se retiró la suspensión viral y se colocó la capa de cubierta. Las bandejas fueron nuevamente colocadas en la incubadora a 37°C o 28°C sin C02 por 24 horas. Una alta humedad fue mantenida en incubadora durante el experimento. Cada celda infectada fue coloreada con una mezcla que contenía formaldehido 10 %, solución de cristal violeta 5 %, agua destilada 85 %. La solución stock de cristal violeta se preparó disolviendo 1 gramo de cristal violeta en 100 ml de alcohol etílico. Después de colorear por una noche las bandejas fueron lavadas con agua corriente secadas y examinadas. Morfología de Placa Tamaño: La medida del diámetro de todas las placas fue hecha por observación de bandejas coloreadas utilizando un micrómetro ocular. El promedio de tamaño de placa de cada aislamiento fue calculado en base a la observación de 100 placas. Para cada aislamiento se hicieron histogramas de la distribución del tamaño de placa. La descripción de las placas se hizo a las 24 horas de incubación. La posible relación entre el tamaño de placa y la virulencia para ratones fue calculada por regresión lineal, coeficiente de correlación y coeficiente de determinación. Títulos: Los títulos fueron calculados en base al promedio de recuento en cuatro celdas por dilución y representan los promedios de dos determinaciones independientes. Pruebas de la letabilidad para ratón tanto de los aislamientos New Jersey como Indiana, fueron hechos por titulación en ratones de diferentes edades y por diferentes vías de inoculación. RESULTADOS Promedio de tamaño de placa: Para los aislamientos Ind. bajo cubierta de agar o goma no hubo diferencia en el promedio de tamaño de placa de 28°C y 37°C (Tablas 1 y 2). Se observó que el tamaño de la placa de una cepa específica bajo una cubierta y temperatura determinada, no predice el tamaño bajo otras condiciones. En los aislamientos N.J. bajo cubierta de agar (Tablas 3 y 4), se observó relación entre el promedio del tamaño de la placa a las dos temperaturas, pero ninguna relación de estos tamaños de placas con el promedio de su tamaño bajo cubierta de goma: 12 de 16 aislamientos bajo cubierta de goma (no siempre las mismas que bajo cepa de agar,) mostraron promedios de tamaño de placa mayores a 28°C que a 37°C. Las cepas con promedios menores de tamaño de placa bajo su cubierta de agar fueron también las más pequeñas bajo cubierta de goma. Distribución de tamaño de placa: El grado de variabilidad encontrado en el promedio de tamaño de placa se expresa en la varianza (Tablas 1, 2, 3 y 4). Bajo cepas de agar y goma la diversidad fue mayor a 37°C que a 28°C para los aislamientos, excepto para los N° 1 -6652 y 1-6653, los cuales mostraron una mayor diversidad a 28°C que a 37°C (Fig. 1 ). Entre los aislamientos N.J. la diversidad de tamaño de placa fue mayor bajo cubierta de agar en cada una de las temperaturas estudiadas. Hubo una tendencia hacia una mayor diversidad de tamaño de placa en las cepas Ind. que las N.J. bajo goma y agar a 37°C y a 28°C. La variabilidád aumentada (Fig. 1 y 2) de la mayoría de las cepas sugirió la presencia de placas que se diferenciaban en su respuesta a inhibidores, encontrado en el agar o en la goma. Cinco de 16 cepas de N.J. (1-6906, 1-6922, 1-7047, 1-7120, 1-7312) no exhibieron aumento de la varianza bajo cepa de agar a 37°C y a 28°C, al igual que cuatro de los aislamientos Ind. (1-6048,1-7120, 1-6922 y 1-6906). Entre los aislamientos N.J. estudiados a 37°C, bajó
cubierta de goma, fue evidente la heterogenicidad en morfología
en 3 de 14 (21 %) de ellos. Bajo cubierta de agar se presentó
heterogenicidad en 8 de 14 aislamientos (57 %). A 28°C fue
observada heterogenicidad en 2 de 14 (14 %) de los aislamientos
estudiados bajo goma o agar. Bajo cubierta de goma, 3 de 6 (50 %)
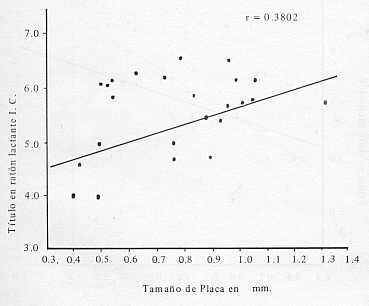
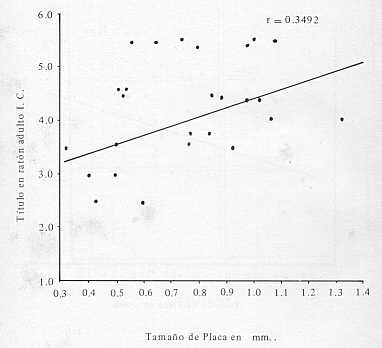
de los aislamientos Ind. mostraron Rango en el tamaño de placa: El rango en el tamaño de placa dependió de la cubierta de soporte utilizada, de la temperatura de incubación y del serotipo, e independiente del promedio del tamaño de placa. El mayor rango de tamaño de placa fue observado para N.J. bajo cubierta de agar a 28°C (rango 0,1 mm, promedio de tamaño 0,76 mm); el segundo tamaño de placa en orden decreciente fue para Ind. bajo cubierta de agar a 28°C (rango 0,89 m m promedio de tamaño 0,95 mm). El tercer rango fue observado bajo cubierta de goma para NJ. a 37°C (rango 0,77 mm, promedio de tamaño 0,4 mm). El rango más pequeño y el segundo más pequeño fueron ambos para Ind. bajo cubierta de goma (rango 0,31 mm promedio de tamaño 0,52 mm) a 37°C y un rango de 0,18 mm, con promedio de tamaño 0,5 mm , a 28°C, la placa más pequeña fue observada bajo cubierta de goma (0,21 mm); para Ind. a 37°C la placa más grande fue (0,14 mm), observada bajo agar. Tamaño de placa y Virulencia: El promedio de tamaño de placa se relacionó con virulencia en ratones lactantes y adultos inoculados vía intracerebral (Fig. 3 y 4). Las cinco cepas de N.J. con los mayores promedios de tamaño de placa (0,13 a 0,94 mm), a 28°C y (0,1 mm a 0,89 mm), a 37°C, mostraron títulos en ratones lactantes que variaron de 6,5 a 5,3 DL50, y en ratones adultos de 5,4 a 4,4 DL50. Las cinco cepas N.J. con los promedios de placa más pequeñas (0,5 a 0,6 mm) basados en un promedio ambas temperaturas, mostraron títulos de 3,9 a 5,DL50 en ratones lactantes y 2,9 a 4,5 DL50 en ratones adultos. El tiempo promedio de vida de los ratones que recibieron los virus que produjeron las placas más grandes tendió a ser más corto que para aquellos inoculados con virus de placa pequeña. Para aislamientos Ind., el promedio de tamaño de placa bajo cubierta de agar a 28°C, presentó una relación inversa con la virulencia en ratones lactantes y adultos inoculados vía intracerebral (Fig. 4). Las tres cepas Ind. con los mayores promedios de placa 1,2 mm (rango 1,0 a 1,4 mm) mostraron en ratones lactantes títulos que variaron entre 2,1 a 5,6 DL50. Las otras cepas de Ind. con los promedios de placa más pequeños 0,8 mm, (rango de 0,7 a 0,9) mostraron en ratones lactantes títulos; que variaron de 6,0 a 6,9 DL50. Entre estos dos grupos no se observó a 37°C diferencia de tamaño de placa. La relación entre el promedio de tamaño de placa de aislamiento N.J y el título en ratones lactantes, está dado por el coeficiente de correlación r =0,380 y el coeficiente de determinación r2 = 14,45 %; con ratones adultos r = 0,349 y r2 = 12,23 %. La relación entre tamaño de placa y la virulencia de los aislamientos Ind. en ratón fue de: r=-0,274 y r2 -8,77 % Título. Ni la capa de cubierta, ni la temperatura de
incubación mostraron un efecto significativo en los promedios de los títulos
(Tablas
5 y 6). En general hubo una buena correspondencia entre los
títulos
DISCUSIÓN La mayoría de las cepas fueron heterogéneas; después de 24 horas de incubación aparecieron 2 ó 3 tipos de placas, morfológica mente diferentes, algunas veces fue necesario más de un sistema para demostrar esas diferencias; De acuerdo a la distribución del tamaño de placa casi todos los aislamien tos estudiados revelaron poblaciones ge néticamente mezcladas, indicando que la variabilidad en el tipo de placa de la E. V. so bre el segundo cultivo de células, que la diversidad gen ética puede ser de un carácter común en la naturaleza. Se han descrito dos categorías de placa (grande 5 a 6 m m y pequeña 2 a 3 mm) basados en su tamaño después de 2 a 4 días de su incubación (34, 15, 22). Gómez y Vieira ( 10) hallaron sólo pequeñas diferencias en tamaño de placas producidas por Ind. 1 e Ind. 2 y placas comple tamente diferentes para Ind. 3. Además del uso de diferentes condicio nes de crecimiento, la amplia heterogenicidad en tamaño de las placas y de la morfología en nuestro estudio podría ser por el tiempo de ob servación. Todas las características pueden colocarse en un continuum en vez de formar varios grupos diferentes. Los resultados de otros in vestigadores son variables. Gómez y Vieira ( 10) y Lauerman (1) han descrito aislamientos de E. V. con placas de un solo tamaño y otros continuum de ellas. La virulencia para ratones de aquellas cepas del virus, N.J. formadoras de placas grandes, tienen un paralelo en muchos otros virus, particularmente en poliovirus (33,25), y Newcastle (7). En cambio la virulencia de las variantes del virus Ind. formadoras de placas pequeñas, ofrece muy pocos paralelos especialmente en arbovirus (Tahyna virus) ( 17). Lauerman ( 15 ), usando otras cepas del virus Ind. y un tiem po de incubación más prolongado observó clones de placa pequeña más virulenta para cobayos. Los virus N.J. e Ind. que crecen en cultivos celulares, difieren en dos aspectos fundamentales: 1) Los aislamientos Ind. crecen mejor a 28°C. que los aislamientos N.J. 2) La virulencia para ratón de los cultivos Ind. está relacionada con placas de tamaño pequeño, mientras que para los virus N.J. existe relación con placas de tamaño grande. La temperatu ra óptima para la producción de placas ha sido determinada para algu nos arbovirus y myxovirus (24) herpes virus ( 13 ), del virus de New-Castle (3). Además del factor medio ambiental que puede modificar el tamaño de la placa, la habilidad de producir una placa de determina do tamaño depende del comportamiento biológico. La rata a la cual un virus es liberado de una célula infectada es lenta para mutantes de placa pequeña del virus del sarampióm (23) del exantema vesicular (20), y del tipo 5 de adenovirus ( 14 ). También se han reportado dife rencias en la rata de síntesis viral y su correlación con tamaño de pla ca. Los clones de placas grandes del virus de la influenza A2, tienen una rata más alta de crecimiento (12). Se han encontrado diferencias en ratas de adsorción para clones de virus derivados de poblaciones paren tales para el virus Coxackie B4 (5) y para el aislamiento Herts del virus de Newcastle (27). Estudios de clones de placas grandes y pequeñas de la cepa de San Juan del virus Ind. han mostrado que dichos clones no se diferencian significativamente en adsorción sobre células CC y L, ni en liberación de células; los estudios sugieren diferencias en sen sibilidad y producción de interferón y en una rata de crecimiento au mentada en los clones de placas grandes. Es posible que la presencia de placas con mayores promedios de tamaño del virus Ind. estudiadas a 28°C, puedan ser explicadas por una producción reducida de interfe rón a una temperatura más baja. Las cepas examinadas sufrieron un solo pase en células BHK21 (des pués de un aislamiento de infecciones naturales en bovinos) tratándose de evitar cambios que pudieran ser inducidos por manipulación en el laboratorio; o por la congelación durante 6 a 12 meses ( -70°C) antes de su uso. El procedimiento de pasaje y preservación fue estandariza do para obtener así cepas con historia similar de aislamiento y de mane jo de laboratorio. Algunos investigadores han usado aislamientos con un número indeterminado de pases en laboratorio, situación que po dría favorecer el reemplazo del virus original por mutantes de difícil sobrevivencia en la naturaleza ( 18). Las condiciones de conservación bajo las cuales el inóculo es mantenido puede influenciar en la super vivencia de algunas placas (21 ). Por estas razones la historia de pasajes y mantenimiento de todas las cepas fue idéntica. No se purificaron los aislamientos por el clonaje. Era deseable man tener la variabilidad intrínseca a cada aislamiento y evitar el riesgo de un selección artificial de una variante que pudiese constituir solamente una mínima proporción de la población viral total. Tampoco fueron estudiados clones derivados de aislamien tos, aunque el virus ha sido clonado varias veces por otros investigadores (34, 15, 26). Sin embargo, los virus heterogéneos usados fueron bastante consis tentes en su habilidad de dar títulos reproducibles en ratones y en cultivos de células. Para estudios de diferencias en tre cepas basadas en la morfología de tamaño de placa, la cubierta de agar permite una mejor información que la obtenida bajo la de goma, pero para la titulación del virus o del an tisuero, la cubierta de goma es más fácil de manejar y permite títulos reproductibles. SUMMARY Six Indiana and 16 New Jersey isolates were studied in BHK21 monolayer cultures. Two differen t temperatures (28°C and 37°C) and two different overlays (agar and gum) were used in the experiment. The plaque titer of strains was not affected by temperature and overlay used. The mean plaque size did not differ at the two temperatures stu died but did differ under the two overlays at the two temperatures. While the plaque sixe of individual strains varied with the temperature a relationship existed under agar but not under gum overlay. Distribu tion in variability of plaque size as revealed a histogram suggests hete rogeneity of the population in most strains that could be established by cloning plaques bases on size and morphology . Strains of New Jersey virus having large size plaques appeared to be more virulent for mice than those having small plaques. The reverse was true for Ind. viruses, the small plaque variant of these viruses appeared to be more virulent. BIBLIOGRAFÍA 1. ANDREWS, C. and PEREIRA, H.G. Vesicular Stomatitis. In: Viruses of Vertebrates. Williams and Wilkins Co., Baltimore. 2ed. ed. 1972. pp. 197- 204. 2. BACHRACH, K.L.; CALLIS, J.J. and HESS. Vesicular Stomatitis Virus Tissue Culture and Cell Suspensions. Proc. Soc. Exp. Biol. Med.: 177- 180.1956. 3. BARON, S. Relationship of Interferon and Temperature to Virulence of Newcastle Disease Virus. Newcastle Dis.Virus as an Evolving Pathogen. Univ. of Wisconsin Press, Madison, 1964. pp.205-220. 4. BERGOLD, G.H. and MAZZALI, R. Plaque Formation by Arbovirus. J. Gen. Virol. 2: 272- 284. 1968. 5. CHAPLIN, M. and DUBES G.R. Triptophan-requiring Mutant of Polyvirus. J. lnfect. Dis. 110: 210-219.1962. 6. COOPER, P.D. The Plaque Assay of Animal Viruses. Adv. Virus Res. 7:319 -37b. 1961. 7. ESTUPIÑAN, J. and HANSON, R.P. Methods of Isolating six mutants Classes from the Hickman strain of Newcastle Disease Virus. Avian Dis. 15: 798- 804. 1971. 8. FEDERER, K.E., BURROW, R,. BROOKSBY, J.B. Vesicular Stomatitis Virus. The Relationship between some Strairis of Indiana Serotype. Res Vet. Sci. 8: 103 - 117. 1967. 9. FIGUEROA, M.E., and RAWLS, W.E. Biological Markers for Differentiation of Herpes Virus strains of oral and genital origen. J. Gen. Virol. 4: 259- 267.1969 10. GOMEZ,.L.G.,VIEIRA, A. Effects of Polyonic Compounds of the Platting Efficiency of some strains of Vesicular Stomatitis Virus. Arch. Gesvirusforch. 34: 223-231. 1971. 11. GUTIERREZ, B.E.; ROCHA, J.; GUTIERREZ, A. Cultivos Celulares en el aislamiento de virus de Efermedades Vesiculares. Rev. ICA. 8: 31- 36.1971. 12. HAN-JIN, C. Plaque Formation of Influenza virus Type A. Acta Microbiol. Sinica 12: 158 - 163.1966. 13. HOGGAN, M.D.; ROIZMAN, B. and TURNER, T .B. The effect of Temperature of Incubation on the Spread of Herpes Simplex Viruses in an Imnune Environmental-cell culture. J. Imnunol. 84: 152-159. 1960. 14. KJELLEN, L.A variant of Adenovirus Type 5. Arch. Ges Virusforch 13: 482-488. 1963. 15. LAUERMAN, L. H. Vesicular Stomatitis in Temperate and Tropical America. Ph.D. Thesis. Univertiy of Wisconsin, Madi son,1967. 16. MAASSAB, H.F. Influenza Virus at 25°C. Nature 5076: 612-613. 1967. 17. MALKOVA, D. Virulence of Tahyna Virus in Mice and its Relation to Thermosensitivitys and character of plaque population Markers Acta Virol. 15: 473-478. 1971. 18. MARTINSON, J.S. Heterogenecity of Foot-and-Mouth Disease Virus Further Studies on Plaque Formation by two Plaque Formation by two Plaque Size Variants. Can. J. Comp. Med. 36: 23-33.1972. 19. MCCLAIN, M .E. and HACKETT, A.J. A Comparative study of the growth of Vesicular Stomatitis Virus Five Tissus Culture Systems. J. Imnunol. 88: 356- 361. 1958. 20. MCCLAIN, M .E.; HACKETT, A.J. and MADIN, S.H. Plaque Morphology and Pathogenecity of Vesicular Exanthema Virus. Nav. Biol. Lab: 127: 1391- 1392. 1958. 21. MCVICAR, J.W., and SUTMPLLER, P. Three Variants of Foot-and-Mouth Disease Virus Type 0: Cell Cultura Characteristics and Antigenic Differences. Am. J. Vet. Res. 33: 1627- 1633. 1972 22. NIZANOV, V .SH., and LASHKEINCH, V .A. Some properties of Large Plaque Mutants of Vesicular Stomatitis Virus Detectable in Cell Culture. Vopr. Virusol. 4: 415 -418. 1973. 23. RAPP, F. Plaque Differentiation and Replication of Virulent and Attenuated Strains of Measles Virus. J. Bact, 88: 1448-1458. 1964. 24. RUIZ - GOMEZ, J. and ISAACS, A. Optimal Temperature for Growth and sensitivity to interferon among different viruses. Virol.19: 1 -7 1963. 25. SABIN, A.B. Properties of attenuated Polioviruses and their behavi cur in Human Beings. In: Cellular Biology , Nucleic Acid and Viruses. N.Y. Academic Science, New York. 1957. pp. 115 -140 26. SCHECHMEUSTER, L.; STRECKFUSS, J. and JOHN, R. ST., Comparative Pathogenecity of Vesicular Stomatitis Virus and its plaque type mutants. Arch. Ges Virusforch. 21: 121-132. 1967. 27. SHLOER, G.M., and HANSON, R.P. Relationship of Plaque Size and Virulence for Chickens and 14 Representative Newcastle Disease Virus Strains. J. Virol. 2: 40- 47.1967. 28. SELLER, R.F.; BURT, L.M.; BURSEELL, R.H. and ARROW. A. L. Studies on Mutants of ECHO 6 Virus. II Isolation from Human Alimentary Tract. Amer. J. Epidem. 81: 333.340. 1965. 29. SODA, K. Plaque Characteristics of Coxakie A7 Virus. Jap. J. Med. Sci. Biol.24: 295-311.1971. 30. TAKEMOTO, K.K., Plaque Mutants of Animal Viruses. Prog. Med. Virol. 8: 313- 348. 31. THOMAR, H.; A comparison of Cocal and Vesicular Stomatitis Virus Serotypes New Jersey and Indiana. Viroligy 31: 323 -328. 1965. 32. TILLES, .J. Enhancement of Vesicular Stomatitis Virus following Adsorption with Poli-ornithine. Proc. Soc. Exp. Biol. 131: 76-81.1969. 33. VOGT., M.; DULBECCO, R. and WENNER, H. A. Mutants of Poliomyelitis Viruses with reduced efficiency of Planting in Acid medium and reduced neuropathogenicity. Virol. 4: 141-155. 1957. 34. WAGNER, R.R.; LEVY, A.H.; SNYDER R.M.; RATCLIFF, G.A. and Hyatt D F. Biologic. Properties of two plaque variantts of Vesicular Stomatitis Virus (Indiana Serotipes). J. Imnunol. 91:112-122. 1963 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||