|
Caña de azúcar, Vol. 05(1): 5-16. 1987 EFECTOS DEL POTENCIAL OSMÓTICO Y LA CONCENTRACIÓN DE P EN EL AGUA DE RIEGO SOBRE EL CRECIMIENTO DE LA CAÑA DE AZÚCAR Antonio Segovia* *UNIVERSIDAD CENTRAL DE
VENEZUELA. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
RESUMEN El objetivo de esta investigación fue estudiar los efectos del potencial osmótico (OP) de la solución nutriente, el tipo de sal, pH y concentración de p en solución en el desarrollo de la caña de azúcar. La variedad de caña , H 50-7209 se cultivó en una mezcla a partes iguales de perlita y vermiculita durante un período de 3 a 5 meses. Durante dos meses las plantas se sometieron a los siguientes tratamientos: combinaciones factoriales de tres OP , 0,05 (testigo), -2,0 y -4,0 bares, establecidos con dos sales (ClNa y SO4Na2); 3 concentraciones de P, 1.7, 2.5 y 3.3 ppm; y, dos niveles de pH, 5.0 y 7.0. La reducción del OP resultó en una reducción significativa del peso seco, el peso fresco y el crecimiento de la yema terminal del tallo. El efecto del OP en estos parámetros del crecimiento fue más acentuado con el SO4Na2 que con el ClNa. Los efectos específicos de los iones SO4 y/o Na se evidenciaron por la mayor reducción del crecimiento observada con el SO4Na2, que con la solución iso-osmótica de ClNa. INTRODUCCIÓN La reducción del crecimiento que experimentan las plantas cuando crecen en condiciones salinas se ha atribuido a: (1) efectos osmóticos y (2) efectos de iones específicos que pueden involucrar: (a) desbalances nutricionales o, (b) efectos tóxicos directos. Los efectos osmóticos están relacionados con la concentración total de sales presentes en solución, independientemente de la especie de planta cultivada. Al aumentar la concentración de sales en la solución disminuye el potencial osmótico (OP), lo cual tiende a reducir la absorción de agua por las raíces de la planta y reduce el crecimiento. Gauch y Wadleigh (1944) observaron que el crecimiento de plantas de fríjol común rojo se reducía cuando el OP de las soluciones disminuía con la adición de CINa, SO4Na2 y CL2Ca a la solución nutritiva básica. Según Bernstein (1961), el desarrollo de las plantas herbáceas en medio salino está gobernado principalmente por efectos osmóticos y en menor grado, por efectos de iones específicos. Heimann (1968) sugirió que los efectos de un exceso de sales en el crecimiento de las plantas, podía modificarse mediante la aplicación razonable de fertilizantes que balancearan a los iones. Sin embargo, los reportes sobre el efecto de la aplicación de P en el crecimiento de plantas cultivadas en condiciones salinas han sido contradictorios. Lunin y Gallatin (1965) observaron que los rendimientos de fríjol aumentaban al aumentar la aplicación de fertilizante P, pero disminuían a medida que se elevaba la salinidad. Por otra parte, Langdale y Thomas (1971) no observaron ningún efecto del P sobre el rendimiento del pasto Bermuda en condiciones salinas. El objetivo de esta investigación fue estudiar los efectos del OP de las soluciones, el tipo de sal, pH y la concentración de P en solución, sobre el peso seco, el peso fresco y el crecimiento apical diario de plantas de caña de azúcar de la variedad H 50-7209. MATERIALES Y MÉTODOS Las diferentes combinaciones que constituyeron los 22 tratamientos que se presentan en el Cuadro 1, se seleccionaron en base a todas las posibles combinaciones factoriales para mantener el experimento bajo control. Los tratamientos se distribuyeron en las bancas de invernadero en un diseño completamente al azar con tres repeticiones. Siembra Se usó caña de azúcar de la variedad H 50-7209. Se cortaron trozos de semilla de una yema dejando 5 cm a ambos lados del entre nudo y se sumergieron en una solución de Benlate (1 g i.a. en 1.600 mI de agua destilada) durante 2 minutos, sembrándose inmediatamente después en recipientes planos conteniendo perlita del tipo agrícola. Los trozos de semilla se agruparon según el diámetro en: grande, mediano y pequeño. Se dejaron crecer las plantas en estos recipientes hasta que aparecieron las raíces de los brotes (aproximadamente 4 semanas). De cada repetición se seleccionaron plantas de altura uniforme, en la misma etapa de desarrollo de raíces. A las 4 semanas de edad las plantas se transplantaron a macetas plásticas de 2.5 galones (una planta por maceta), las cuales estaban llenas de una mezcla a partes iguales de perlita y vermiculita hasta 5 cm del borde superior. Cada maceta tenía 2 ó 3 agujeros a los lados cerca del fondo. Uno de los agujeros se tapó con lana de vidrio para facilitar el drenaje y evitar pérdida del medio, mientras que el o los agujeros restantes se sellaron con cinta adhesiva plástica. Todas las macetas se colocaron en las bancas del invernadero en una plataforma levantada de manera que la solución lixiviada pudiera colectarse en pailas plásticas colocadas debajo de las macetas. Preparación de la solución nutriente Para preparar y guardar las soluciones nutrientes se usaron 22 barriles de metal de 20 galones, forrados con bolsas de polietileno transparente. Cada barril se llenó con 60 litros de agua destilada. Las respectivas soluciones salinas se prepararon de acuerdo a Tanimoto (1969) y se añadieron a los barriles. Como la fuente de P añadida fue PO4H2K, la concentración de K en solución se ajustó siempre que fue necesario, agregando cantidades adicionales de CIK en el tratamiento de CINa y el testigo, y SO4K2 al tratamiento de SO4Na2. Una vez añadidas todas las clases a cada barril, se ajustó el pH al valor deseado. El pH se ajustó a 5 con ácido clorhídrico 0.1 N en el testigo y en el tratamiento de CINa, y con ácido sulfúrico normal en tratamientos de SO4Na2. Para obtener un pH de 7.0, las soluciones se ajustaron con solución 0.1 N de NaOH, tanto en el testigo como en los tratamientos salinos. La composición de la solución se detalla en el Cuadro 2.
Observaciones durante el experimento La concentración de sal necesaria para obtener potenciales osmóticos de -2 y -4 bares se obtuvo de las curvas que relacionan las concentraciones de cada una de las sales en meq/l, con la conductividad eléctrica en mmhos/cm, y la conductividad eléctrica con el potencial osmótico en bares (U.S.S.L. Staff, 1954). Las sales se añadieron a los barriles designados conteniendo la solución nutriente básica a razón de un bar por día. Se hizo en esta forma para permitir que las plantas se adaptaran gradualmente al potencial osmótico menor. La concentración de sales necesaria para reducir en una atmósfera el potencial osmótico de la solución fue de 24 meq/l para el ClNa y de 36 meq/l para el SO4Na2. Los potenciales osmóticos se verificaron midiendo la CE de las soluciones una vez añadidas las sales. Riego A continuación del trasplante las plantas recibieron un riego con agua corriente. Los riegos con las soluciones nutrientes se llevaron a cabo mediante tubos goteros conectados a bolsas plásticas sostenidas dentro de recipientes plásticos de un galón. Estos recipientes se colocaron sobre una plataforma levantada, de manera que el litro de solución nutriente suministrado diariamente a cada maceta pudiera fluir por el tubo gotero a la base de la planta colocada en la parte inferior. Durante 12 días las plantas se regaron diariamente con un litro de la solución nutriente básica antes de iniciar los tratamientos salinos. Estos se impusieron a razón de un bar de potencial osmótico diario. Durante las cuatro primeras semanas del experimento las plantas se regaron con solución nutriente a 1/50 de la usada por Tanimoto. Pero como no era posible detectar diferencias en crecimiento entre el testigo y los tratamientos salinos, se elevó la concentración de la solución a 1/10 de la solución de Tanimoto. Esta solución tenía un potencial osmótico de 0.51 bares según los cálculos hechos a partir del dato de conductividad eléctrica, mediante la ecuación: potencial osmótico (bares)=0.36 x CE en mmhos/cm (U.S.S.L. Staff, 1954). Preparación de los tratamientos salinos Plantas -La tasa de crecimiento apical se registró cada dos días a partir del establecimiento de los tratamientos salinos, según la metodología descrita por Mongelard y Mimura (1971).
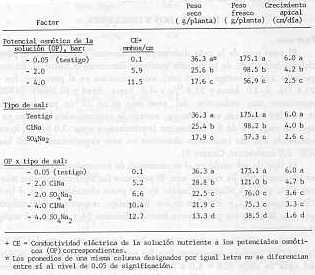
Lixiviado y solución -Se determinó la conductividad eléctrica de los lixiviados una semana después de establecidos los tratamientos salinos y al final del experimento. El lixiviado se obtuvo colectando en ampolletas plásticas los primeros 100 ml de solución que drenaban del fondo de las macetas inmediatamente después del riego. Las CE promedio de los lixiviados fueron 0.12, 5,32 y 11,0 mmhos/cm para los tratamientos con CINa de 0, -2 y -4 bares y 6,82 y 13,3 mmhos/cm en los tratamientos con SO4Na2 de -2 y -4 bares. Las CE promedio de las soluciones nutrientes fueron 0)092, 4,96 y 10,2 mmhos/cm en los tratamientos con CINa de 0, -2 y -4 bares. En los tratamientos con SO4Na2 las CE fueron 6,52 y 12,2 mmhos/cm para potenciales osmóticos de -2 y-4 bares, respectivamente. Los valores teóricos obtenidos mediante la curva de relación entre la CE de cada una de las soluciones salinas y el potencial osmótico (U.S.S.L. Staff 1954 ), indic6 que el testigo y las soluciones con CINa de -2 y -4 bares debían tener CEs de 0,1, 5,2 y 10,4 mmhos/cm. L os valores correspondientes al usar SO4Na2 a potenciales osmóticos de -2 y -4 bares fueron 6,6 y 12,7 mmhos/cm. En la discusión de los resultados se usaron OP de 0, -2 y -4 bares. RESULTADOS Y DISCUSIÓN Peso seco El peso seco de la caña disminuyó linealmente a medida que el potencial osmótico (OP) de la solución nutriente disminuyó (Cuadro 3). En comparación con el testigo (-0.05 bar), esta reducción en el peso seco fue de 29,4 % a -2.0 bares y 51,9 % a -4,0 bares. Syed y El Swafy (1972a) reportaron una reducción a el peso seco de un 23 % para la variedad H 50-7209 sembrada en el campo, cuando la concentración de sales en el agua de riego era de 8.0 mmhos/cm (equivalente a unos -3.0 bares), lo cual concuerda con los resultados obtenidos en este experimento a -2.0 bares (CE 5.9 mmhos/cm, Cuadro 3). El tipo de sal usado en el experimento de invernadero influyó también en la acumulación de materia seca. El peso seco fue significativamente mayor con CINa que con SO4Na2 (Cuadro 3). Los pesos obtenidos a -2 y -4 bares, CINa, fueron 78,1 y 59,0 % de los del testigo, respectivamente; mientras que con SO4Na2 los pesos secos fueron solamente 64 y 36 % del testigo, respectivamente. Estos resultados contrastan con los obtenidos por Syed y El Swafy (1972a), quienes reportaron que las concentraciones altas de SO4Na2 del agua de riego (CE = 6.0 a 8.0 mmhos/cm) inhibieron menos el crecimiento (peso seco) que el CINa en la variedad H 50-7209. Ellos atribuyen estos resultados a posibles efectos beneficiosos del SO4 en cuanto a la disponibilidad del fosfato en el suelo. Se concluye que la mayor inhibición del crecimiento de la caña con el SO4Na2 en relación al desarrollo obtenido con CINa en la prueba de invernadero se debió a efecto específico del ión, ya que los dos tipos de sal usados eran iso-osmóticos. Este efecto específico pudiera atribuirse al mayor efecto detrimental sobre el crecimiento del SO4 o a la mayor concentración de Na en la solución de SO4Na2 que en la de CINa (72 y 144 versus 24 y 48 meq/Na/1 a -2.0 y -4.0 bares respectivamente). Los efectos del pH en el peso seco de la caña no fueron significativos, aunque éste fue ligeramente menor a pH 7.0 que a pH 5.0, independientemente del OP o del tipo de sal usado (Cuadro 4 ).
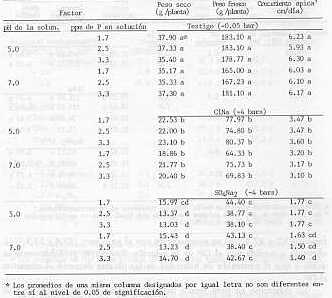
La concentración de P en la solución nutriente no tuvo un efecto significativo en peso seco a cualesquiera de los valores de pH o de potencial osmótico evaluados (Cuadro 5). Resultados similares se han obtenido con otros cultivos. Patel y Wallace (1976) encontraron que un aumento en la concentración de P en la solución (6 a 40 ppm) no afectó significativamente el peso del maíz o del pasto Sudán, a niveles de salinidad entre 6 y 12 mmhos/cm. Peso fresco Los efectos en el peso fresco del potencial osmótico decreciente se muestran en el Cuadro 3. A -2.0 y -4.0 bares el peso fresco de la caña fue un 56.3 y 32,5% del peso testigo, respectivamente. La mayor reducción del peso fresco (43,7 y 67,5 %) en comparación con el peso seco (29,4 y 15,9%), obtenida a medida que el OP de la solución disminuyó, probablemente se debió a que el contenido de humedad de las plantas decreció al aumentar el OP.
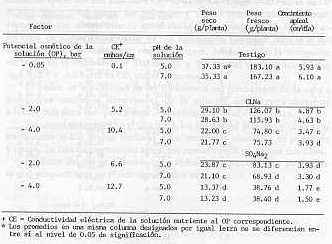
La reducción en peso fresco debido al menor OP de la solución fue mayor cuando se usó CINa (Cuadro 3). El sulfato de sodio redujo el peso fresco en un 56,6% a los primeros -2.0 bares de OP, mientras que la reducción entre -2.0 y -4.0 bares fue de 49% (Cuadro 3). El peso fresco fue significativamente más alto a pH 5.0 que a pH 7.0 en el testigo (-0.05 bares) ya -2.0 bares de OP con ambos tipos de sales, (Cuadro 4), pero estas diferencias desaparecieron al nivel más bajo de OP . El mayor crecimiento obtenido a OPs más altos (0.05 y -2.0 bares) pudiera atribuirse en parte a una mayor absorción de agua y nutrientes con el pH 5.0 que con pH 7.0, debido al mayor desarrollo de raíces. Thorup (1969) reportó que el desarrollo radical y la absorción de agua por plantas de tomate cultivadas en solución nutriente fue mayor a los pH más bajos ( 4.7 a 5.4) que a los más altos (pH 7.0). Al parecer el crecimiento se inhibió tan severamente a -4.0 bares de presión que el efecto del pH se enmascaró.
El aumento de 1,7 a 3,3 ppm en la concentración de p de la solución nutriente no afect6 significativamente el peso fresco a los potenciales altos (testigo) o bajos (-4,0 bares) sin importar el pH de la solución (Cuadro 5). La poca respuesta en peso fresco obtenido al aumentar el P se debió posiblemente a que las 1,7 ppm de p de la solución nutriente eran adecuadas para el crecimiento de la caña. Crecimiento apical diario Al disminuir el potencial osmótico de la solución nutriente se redujo significativamente el crecimiento apical diario (Cuadro 3). La tasa de crecimiento apical fue tan sólo un 69,6 % de la del testigo a -2.0 bares de OP y 41,1 % a 4.0 bares. Bartholomew y Tianco (comunicación personal) reportaron que el crecimiento apical diario de la variedad H 59-3775 en soluciones de CINa fue un 82 y 64 % en relación al testigo, a -2.0 y -4.0 bares de potencial osmótico, respectivamente, mientras que la elongación del tallo en el cultivar NCo 310 fue 81 y 70 % del crecimiento del testigo, a -2.0 y -4.0 bares de OP, respectivamente. El orden de sensibilidad de los parámetros del crecimiento de la caña a potenciales osmóticos decrecientes de la solución salina, particularmente a los OP más altos fue: peso fresco > crecimiento apical >peso seco. Tal como se muestra en el Cuadro 3, los efectos del SO4Na2 y CINa en el crecimiento apical fueron similares a los resultados obtenidos en peso seco y fresco. La tasa de crecimiento apical fue menor con SO4Na2 que con CINa. El efecto del pH en el crecimiento apical fue imperceptible y por su parte el p tampoco tuvo un efecto significativo en éste. EFFECTS OF OSMOTIC POTENCIAL AND P CONCENTRATION IN THE IRRIGATION WATER ON THE GROWTH OF SUGARCANE ABSTRACT The objetive of this research was to study the effects of solution osmotic potential (OP), salt type, solution pH and the concentration of P in solution on the growth of sugarcane. Sugarcane variety H50-7209 was grown in a mixture of equal parts of perlite and vermiculite for 3-5 months. The treatments which were imposed for 2 months, consisted of factorial combinations of three OP: 0.05 (Control), -2.0 and -4.0 bars stablished with 2 salts, NaCI and Na2SO4; 3 P concentrations: 1.7, 2.5 and 3.3 ppm; and 2 pH levels: 5.0 and 7.0. Decreasing OP resulted in a significant reduction in dry weight, fresh weight and spindle growth. The effect of OP on these growth parameters was greater with Na2S04 than with NaCI. Evidence of specific ion effects of SO4 and/or Na was provided by the greater reduction in growth with Na2SO4 than with isosmotic concentration of NaCI. BIBLIOGRAFÍA 1. BERNSTEIN, L. 1961. Osmotic adjustment of plants to saline media I. Steady state. Amer. J. Bot. 48: 909-918. 2. GAUCH, H. G. and C. H. WADLEIGH. 1944. Effects ofhigh salt concentration on growth of bean plants. Bot. Gaz. 105: 379-387. 3. HEIMANN, H. 1958. Potassium symp. International Potassium Inst., Berne. 4. LANGDALE, G. W. and J. R. THOMAS. 1971. Soil salinity effects on absorption of nitrogen, phosphorus, and protein synthesis by coastal berrnuda grass. Agron. J. 63: 708-711. 5. LUNIN, J. and M. H. GALLATIN. 1965. Salinity-fertility interactions in relation to the growth and composition of beans. I. Effects of N, P, and K. II. Varying levels of N and P. Agron. J. 4; 339-345. 6. MONGELARD, J. C. and L. MIMURA. 1971. Growth studies on sugar cane plant. I. Effects oftemperature. Crop Sci. 11: 795-800. 7. PATEL, P. and A. WALLACE. 1976. P fertility and mixed salinity on the growth and Ca, Mg, Na, P and cl concentrations of tomato, corn and sudan grass on sand culture. Commun. Soil Sci. and Plant Anal. 7: 375-385. 8. SYED. M. M. and S. A. EL-SWAIFY. 1972. Effects of saline water irrigation on NCo 310 and H 50-7209 cultivars of sugar cane. I. Growth parameters. Trop. Agric. (Trinidad) 49: 337-346. 9. TANIMOTO, T. T. 1969. Differential physiological response of sugar cane varieties to osmotic pressures of saline media. Crop Sci. 9: 683-688. 10. THORUP , J. T. 1969. pH effects on root growth and water uptake by plants. Agron. J. 61: 225-189. 11. U. S. SALINITY LABORATORY STAFF. 1954. Diagnosis and improvement of saline and alkali soils. U.S. Dept. Agr. Handbook 60. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||